- Recherche
-
VOUS ÊTES
- Membre de la communauté
- Futur étudiant
- Étudiant
- Professeur
- Diplômé
- Média
- Conseillers en orientation
- Retraité de l’INRS
- Nous joindre
- Nouvelles
- Emplois
- EN
-
Les Études
Nous formons la relève en recherche, capable d'innovation scientifique, sociale et technologique.
-
La recherche
Nous trouvons des solutions par la recherche interdisciplinaire, en collaboration avec nos partenaires.
-
L'INRS
Nous contribuons au développement économique, social et culturel du Québec.
La saison des rhumes est de retour et on se demande pourquoi on peut avoir ce virus à répétition, hiver après hiver. Comment se fait-il qu’on ne soit jamais immunisé contre le rhume?
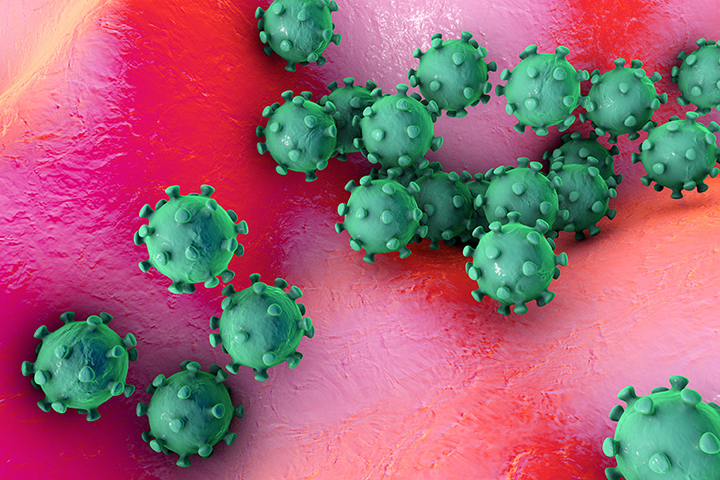
llustration Adobe stock
Le professeur Pierre Talbot de l’INRS connaît depuis longtemps la grande variabilité de la famille des coronavirus responsables du rhume commun, mais aussi de nombreuses autres infections dont des affections neurologiques. Il a participé, avec son associé de recherche Marc Desforges, à une étude publiée dans la revue Nature Communications rapportant comment un virus de cette grande famille s’adapte et évolue pour être toujours plus efficace à infecter son hôte sans se faire freiner par le système immunitaire.
Petites sphères hérissées d’épines, les coronavirus sont sous haute surveillance par la santé publique puisqu’ils franchissent la barrière des espèces et certains ont un potentiel élevé de mortalité. Au cours des dernières décennies, le SRAS et le MERS ont émergé de cette famille de virus. Cette capacité à s’adapter à de nouveaux environnements aurait quelque chose à voir avec les épines à la surface du virus, plus particulièrement à une petite région stratégique des protéines qui les constituent.
Assemblage de protéines-S (pour spike ou épine), les épines exhibent une région qui permet au virus de s’agripper aux cellules de l’hôte. La région DLR (domaine de liaison au récepteur), qui initie l’interaction entre la cellule et le virus, est essentielle pour mener efficacement une infection. Elle est cependant aussi la cible des anticorps qui neutralisent le virus et permettent au système immunitaire de l’éliminer.
Les coronavirus sont donc confrontés, d’un point de vue évolutif, à un problème. Ils ne peuvent pas infecter les cellules sans leur DLR et doivent le garder accessible pour qu’il s’agrippe aux cellules. D’autre part, pour éviter que le virus soit détecté par le système immunitaire, il vaudrait mieux dissimuler ce fameux DLR puisqu’il est la cible d’anticorps.
Le mécanisme développé fait un compromis qui participe au succès des coronavirus. Le DLR comprend trois régions qui varient grandement d’une souche à une autre. Cette variation fait en sorte que les anticorps ne reconnaissent pas une nouvelle souche, alors que le DLR conserve – voire améliore – son affinité avec la cellule à infecter. De plus, le DLR est tantôt visible, tantôt camouflé.
Pour parvenir à cette proposition, un groupe de chercheurs dont fait partie le professeur Talbot a étudié l’alpha-coronavirus HCoV-229E et, plus particulièrement, l’interaction entre son DLR et l’aminopeptidase N (APN), la protéine à laquelle il s’attache sur les cellules hôtes. Ils ont figé le complexe de ces deux protéines sous forme de cristal, puis analysé leur structure.
En regardant de près la structure du DLR, l’équipe a identifié trois boucles allongées qui sont responsables de la liaison à l’APN. Comme le confirme l’analyse des virus qui ont circulé au cours des cinquante dernières années, ce sont presque exclusivement ces boucles qui varient.
Les expériences montrent que les changements observés dans les boucles modulent l’affinité du DLR pour l’APN. Les variantes qui ont une plus grande affinité ont probablement aussi une plus grande efficacité d’infection, ce qui les favorise. D’ailleurs, six classes de HCoV-229E se sont succédé au fil des années, dont le RBD a une affinité croissante pour APN.
Cette découverte améliore la compréhension de l’évolution des coronavirus et pourra mener à des analyses similaires dans les autres types de coronavirus. Bien qu’il reste de nombreux éléments à élucider, le DLR semble être un élément important à surveiller pour suivre les virus dans leurs adaptations évolutives et pour identifier leur potentiel d’infection.
À propos de cette publication
Les résultats de cette étude sont publiés dans l’article « Receptor-binding loops in alphacoronavirus adaptation and evolution » (DOI : NCOMMS-17-12455) paru dans Nature Communications. Alan H.M. Wong, Aidan C.A. Tomlinson, Dongxia Zhou, Malathy Satkunarajah, Kevin Chen, Chetna Sharon, Marc Desforges, Pierre J. Talbot et James M. Rini ont participé à cette recherche qui a bénéficié du soutien financier des Instituts de recherche en santé du Canada et des Chaires de recherche du Canada.
Découvrez notre dossier
Vous aimerez aussi
Partager